Thành phần hóa học chính của đất sét là Al₂O₃. 2SiO₂. 2H₂O. Hãy tính phần trăm khối lượng của nhôm trong hợp chất trên.
\(\%Al=\dfrac{27.2}{102+60.2+18.2}.100\%\approx20,93\%\)
Đúng 2
Bình luận (0)
Thành phần chính của đất sét là Al 2 O 3 .2SiO 2 .2H 2 O. Phần trăm khối lượng
của nhôm trong hợp chất trên là bao nhiêu?
Giải thích các bước giải:
M Al2O3.SiO2.2H2O = 198
%mAl = = 27.2.100:198= 27,27%
Xem thêm câu trả lời
Thành phần hoá học chính của đất sét là : Al2O3. 2SiO2.2H2O. Hãy tính phần trăm khối lượng của nhôm trong hợp chất trên.
M Al2O3.2SiO2.2H2O =258
%mAl = \(\dfrac{54.100\%}{258}\)=20,93%
Đúng 1
Bình luận (1)
M Al2O3.2SiO2.2H2O =258
%mAl = 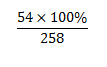
Đúng 1
Bình luận (0)
Calcium carbonate là thành phần chính của đá vôi, có công thức hóa học là CaCO3. Tính phần trăm khối lượng của mỗi nguyên tố trong hợp chất trên
\(PTK_{CaCO_3}=NTK_{Ca}+NTK_C+3.NTK_O=40+12+3.16=100\left(đ.v.C\right)\\ \%m_{Ca}=\dfrac{NTK_{Ca}}{PTK_{CaCO_3}}.100\%=\dfrac{40}{100}.100=40\%\\ \%m_C=\dfrac{NTK_C}{PTK_{CaCO_3}}.100\%=\dfrac{12}{100}.100=12\%\\ \%m_O=100\%-\left(\%m_{Ca}+\%m_C\right)=100\%-\left(40\%+12\%\right)=48\%\)
Đúng 0
Bình luận (0)
Đốt cháy hỗn hợp bột của kim loại magie và nhôm cần 33,6 lít khí oxi ở đktc. Biết khối lượng nhôm trong hỗn hợp là 2,7 gam. Hãy tính thành phần phần trăm khối lượng của hai kim loại trong hỗn hợp trên.
PTHH: \(2Mg+O_2\underrightarrow{t^o}2MgO\) (1)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\) (2)
Ta có: \(\left\{{}\begin{matrix}\Sigma n_{O_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\\n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\Rightarrow n_{O_2\left(2\right)}=0,075\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{O_2\left(1\right)}=1,425\left(mol\right)\) \(\Rightarrow n_{Mg}=2,85\left(mol\right)\)
\(\Rightarrow\%m_{Mg}=\dfrac{2,85\cdot24}{2,85\cdot24+2,7}\cdot100\%\approx96,2\%\)
\(\Rightarrow\%m_{Al}=3,8\%\)
Đúng 1
Bình luận (0)
\(n_{O_2} =\dfrac{33,6}{22,4} = 1,5(mol)\\ n_{Al} = \dfrac{2,7}{27} = 0,1(mol)\\ 2Mg + O_2 \xrightarrow{t^o} 2MgO\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ n_{O_2} = \dfrac{1}{2}n_{Mg} + \dfrac{3}{4}n_{Al}\\ \Rightarrow n_{Mg} = 2,85(mol)\)
Vậy :
\(\%m_{Mg} = \dfrac{2,85.24}{2,85.24 + 2,7}.100\% = 96,2\%\\ \%m_{Al} = 100\% - 96,2\% = 3,8\%\)
Đúng 2
Bình luận (0)
Câu 1: Tính thành phần trăm theo khối lượng của các nguyên tố trong hợp chất: a)Al2O3 b)C6H12O Câu 2:Một hợp chất có thành phần các nguyên tố là 5,88% H và 94,12% S , khối lượng mol của hợp chất là 34 gam .Tìm CTHH của hợp chấy trên
Câu 1:
a) Al2O3:
Phần trăm Al trong Al2O3: \(\%Al=\dfrac{27.2}{27.2+16.3}.100=52,94\%\)
Phần trăm O trong Al2O3: \(\%O=100-52,94=47,06\%\)
b) C6H12O:
Phần trăm C trong C6H12O: \(\%C=\dfrac{12.6}{12.6+12+16}.100=72\%\)
Phần trăm H trong C6H12O: \(\%H=\dfrac{1.12}{12.6+12+16}.100=12\%\)
Phần trăm O trong C6H12O : \(\%O=100-72-12=16\%\)
Câu 2:
\(m_H=\dfrac{5,88.34}{100}\approx2\left(g\right)\)
\(m_S=\dfrac{94,12.34}{100}=32\left(g\right)\)
\(n_H=\dfrac{m}{M}=\dfrac{2}{1}=2\left(mol\right)\)
\(n_S=\dfrac{m}{M}=\dfrac{32}{32}=1\left(mol\right)\)
⇒ CTHH của hợp chất: H2S
Đúng 1
Bình luận (0)
Thành phần phần trăm về khối lượng của nguyên tố kim loại M trong hỗn hợp MCl2 và MSO4 là 21,1%. Thành phần phần trăm về khối lượng của nguyên tố clo trong hỗn hợp trên là
A. 33,02%
B. 15,62%
C. 18,53%
D. 28,74%
Giải thích: Đáp án B
Xét trong 1 mol hỗn hợp :
- Gọi x là số mol MCl2 thì số mol của MSO4 là 1 - x
- Số mol của M : x + 1 - x = 1 mol
=> Khối lượng hỗn hợp là : (M + 71)x + (M + 96)(1 - x) = M + 96 - 25x
Phần trăm khối lượng M trong hỗn hợp là :
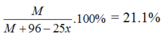
Ta có 0 < x < 1 => 18.9 < M < 25.7 => M = 24 (Mg)
=> x = 0.25 mol
=> khối lượng hỗn hợp là (24 + 71). 0,25 + (M + 96)(1 – 0,25) = 113.75g
=> %Cl = 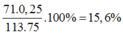
Đúng 0
Bình luận (0)
Thành phần phần trăm về khối lượng của nguyên tố kim loại M trong hỗn hợp MCl2 và MSO4 là 21,1%. Thành phần phần trăm về khối lượng của nguyên tố clo trong hỗn hợp trên là A. 33,02%. B. 15,60%. C. 18,53%. D. 28,74%.
Đọc tiếp
Thành phần phần trăm về khối lượng của nguyên tố kim loại M trong hỗn hợp MCl2 và MSO4 là 21,1%. Thành phần phần trăm về khối lượng của nguyên tố clo trong hỗn hợp trên là
A. 33,02%.
B. 15,60%.
C. 18,53%.
D. 28,74%.
Câu 1: Thành phần phần trăm về khối lượng của nguyên tố Fe trong hợp chất Fe3O4 là:A. 72,4%B. 68,8%C. 76%D. 62,5%Câu 2: Hợp chất X có khối lượng mol phân tử là 232 g/mol, thành phần phần trăm khối lượng của Fe là 72,41%, còn lại là của O. Công thức hóa học của X làA. Fe3O4.B. FeO.C. Fe3O2.D. Fe2O3.Câu 3: Trong 1 mol phân tử FeCl3 có bao nhiêu gam nguyên tử clo?A. 71,0 gam.B. 35,5 gam.C. 142,0 gamD. 106,5 gam.Câu 4: Có bao nhiêu mol nguyên tử O trong 1 mol phân tử N2O5?A. 2 mol.B. 4 mol.C. 5 mo...
Đọc tiếp
Câu 1: Thành phần phần trăm về khối lượng của nguyên tố Fe trong hợp chất Fe3O4 là:
A. 72,4%
B. 68,8%
C. 76%
D. 62,5%
Câu 2: Hợp chất X có khối lượng mol phân tử là 232 g/mol, thành phần phần trăm khối lượng của Fe là 72,41%, còn lại là của O. Công thức hóa học của X là
A. Fe3O4.
B. FeO.
C. Fe3O2.
D. Fe2O3.
Câu 3: Trong 1 mol phân tử FeCl3 có bao nhiêu gam nguyên tử clo?
A. 71,0 gam.
B. 35,5 gam.
C. 142,0 gam
D. 106,5 gam.
Câu 4: Có bao nhiêu mol nguyên tử O trong 1 mol phân tử N2O5?
A. 2 mol.
B. 4 mol.
C. 5 mol.
D. 3 mol.
Câu 5: Khối lượng của Fe trong 92,8 g Fe3O4 là
A. 25,6 g.
B. 67,2 g.
C. 80 g.
D. 10 g.
Câu 1: Thành phần phần trăm về khối lượng của nguyên tố Fe trong hợp chất Fe3O4 là:
A. 72,4%
B. 68,8%
C. 76%
D. 62,5%
Câu 2: Hợp chất X có khối lượng mol phân tử là 232 g/mol, thành phần phần trăm khối lượng của Fe là 72,41%, còn lại là của O. Công thức hóa học của X là
A. Fe3O4.
B. FeO.
C. Fe3O2.
D. Fe2O3.
Câu 3: Trong 1 mol phân tử FeCl3 có bao nhiêu gam nguyên tử clo?
A. 71,0 gam.
B. 35,5 gam.
C. 142,0 gam
D. 106,5 gam.
Câu 4: Có bao nhiêu mol nguyên tử O trong 1 mol phân tử N2O5?
A. 2 mol.
B. 4 mol.
C. 5 mol.
D. 3 mol.
Câu 5: Khối lượng của Fe trong 92,8 g Fe3O4 là
A. 25,6 g.
B. 67,2 g.
C. 80 g.
D. 10 g.
Đúng 1
Bình luận (0)
Một hợp kim nhẹ gồm 60 phần trăm nhôm và 40 phần trăm magie . Tìm khối lượng riêng của hợp kim biết rằng các tỉ lệ trên tính theo khố lượng . Biết khối lượng riêng của nhôm là D1=2700kg/m khối của magie là D2=1740kg/m khối
Gọi m1 là khối lượng Nhôm trong hợp kim
Gọi V1 là thể tích Nhôm trong hợp kim
=> m1 = D1×V1 = 2700×V1
Gọi m2 là khối lượng Ma-giê trong hợp kim
Gọi V2 là thể tích ma-giê trong hợp kim
=> m2 = D2×V2 = 1740×V2
một hợp kim nhẹ gồm 60% nhôm và 40% ma-giê
=> m1 = 60% (m1 + m2)
=> 100m1 = 60(m1 + m2)
=> 4m1 = 6m2
=> m1 = 1,5m2
=> 2700×V1 = 1,5×1740×V2
=> 2700×V1 = 2610×V2
=> V1 = 0,967×V2
Khối lượng riêng của hợp kim:
Dhk = (m1 + m2)/(V1 + V2)
Do m1 = 2700×V1 và m2 = 1740×V2
=> Dhk = (2700×V1 + 1740×V2 ) / (V1 + V2)
Do 2700×V1 = 2610×V2 & V1 = 0,967×V2
=>Dhk = (2610×V2 + 1740×V2 ) / (0,967×V2 + V2)
=>Dhk = 4350×V2 / 1,967×V2
=>Dhk = 4350 / 1,967
=>Dhk = 2211,5 kg/m3
Đúng 0
Bình luận (0)
Ta có \(\dfrac{m_1}{m_2}=\dfrac{60}{40}=\dfrac{3}{2}\Rightarrow m_1=\dfrac{3}{2}m_2\)
\(\Leftrightarrow D_1V_1=\dfrac{3}{2}.D_2.V_2\)
\(\Leftrightarrow2700V_1=2610V_2\)\(\Rightarrow\dfrac{V_1}{V_2}=\dfrac{2610}{2700}=0,967\Leftrightarrow V_1=0,967V_2\)
D = \(\dfrac{m_1+m_2}{V_1+V_2}=\dfrac{\dfrac{5}{2}m_2}{1,967V_2}=\dfrac{\dfrac{5}{2}}{1,967}.\dfrac{m_2}{V_2}=\dfrac{\dfrac{5}{2}}{1,967}.D_2=\dfrac{2500.1740}{1967}\)
= 2211,5kg/m3
Đúng 0
Bình luận (0)


































